Соль
Содержание:
- Двойные и комплексные соли
- Значение морской соли для организма
- Классификация и номенклатура
- Физические свойства соли
- Что такое соль?
- Значение хлорида натрия для организма человека (adsbygoogle = window.adsbygoogle || []).push({});
- Значение хлорида натрия для организма человека
- Классификация соли
- Природные месторождения
- Растворы кислых солей
- Излишек соли в организме
- Польза в хозяйстве
- Определение соли
- Соль и пищеварительная система
- Краткое описание
- Технология добычи
Двойные и комплексные соли
Двойными называют соли, в которых один кислотный остаток соединен с двумя металлами. Например, в составе алюмокалиевых квасцов на один сульфат-ион приходится ион калия и ион алюминия. Составим формулу:
- Запишем формулы всех металлов и кислотного остатка: KAl SO4.
- Проставим заряды: K (+), Al (3+) и SO4 (2-). В сумме заряд катионов 4+, а анионов — 2-. Сокращаем 4 и 2 на 2.
- Записываем итог: KAl(SO4)2 — сульфат алюминия-калия.
Комплексные соли содержат комплексный анион или катион: Na — тетрагидроксоалюминат натрия, Cl — хлорид диамминмеди (II). Подробнее комплексные соединения будут рассмотрены в отдельной главе.
Подведем итог. Формулы солей, так же, как и формулы кислот, содержат в своем составе кислотный остаток. Обязательно в составе соли должны присутствовать катионы металлов или аммония. В формулах кислых или средних солей содержатся катионы Н+ или анионы ОН- соответственно. В комплексных солях катион либо анион представляют собой комплекс из металла и лигандов. Здесь можно прочитать также про химические свойства солей и химические свойства кислот.
Значение морской соли для организма
Соль, добываемая из морских глубин, обладает уникальными качествами. В лабораторных условиях ученые до сих пор не смогли вывести ее аналог, несмотря на то, что состав кристалла давно известен. Эзотерики утверждают, что соль, получаемая из морской воды, обладает большой силой природной энергии, которая наполняет организм человека гармонией и здоровьем .
Испокон веков хлористый натрий использовали как природный консервант, увеличивающий срок годности продуктов. На его основе готовили составы для продления молодости и красоты.
Влияние соли на организм человека:
- регулирует и поддерживает в пределах нормы водный баланс, натрий-калиевый ионный обмен;
- избавляет от спазмов гладкой мускулатуры;
- снабжает организм макро- и микроэлементами, в частности натрием;
- успокаивает нервную систему;
- способствует синтезу соляной кислоты;
- тормозит гнилостные процессы в ЖКТ (за счет антисептических свойств);
- ускоряет метаболизм;
- способствует формированию клеточных оболочек, образованию эритроцитов;
- поддерживает нормальный гормональный, липидный обмен, функцию половых желез;
- улучшает состояние кожных покров.
Соль выступает противоаллергическим, дезинфекционным агентом. Ее полезно не только употреблять внутрь, но и использовать наружно в качестве ванн, ингаляций, в составе масок. Так, соляные компрессы под глаза избавляют от мешков, полоскания с добавлением соды снимают воспаления миндалин, а ванночки избавляют от отека ног .
Классификация и номенклатура
Основные классы этой группы веществ были описаны французским химиком и аптекарем Г. Руэлем еще в 1754 году, а по мере развития химии к ним добавились новые. Главный принцип классификации солей основан на том, что при взаимодействии металла и кислоты в ней происходит частичное или полное замещение атомов водорода.
Общие характеристики
Формулы солей всегда образуются одним или несколькими металлами, кислотными остатками и гидроксильными группами. В зависимости от этого все солевые соединения делят на такие классы:
- Средние.
- Кислые.
- Основные.
- Двойные или смешанные.
- Комплексные.
- Кристаллогидраты.
Средними считаются те, у которых все атомы водорода образующей кислоты заменены атомами металла. К такому типу соединений относятся и те, в которых водород замещается одновалентной группой аммония NH4. Согласно принятой номенклатуре, названия этих веществ образуются из латинского названия кислотного остатка и русского названия металла. Кислородосодержащие остатки оканчиваются на «ат», бескислородные — на «ид». Например:
- Na2CO3 — карбонат натрия.
- NaCl — хлорид натрия.
- KNO3 — нитрат калия.
Кислые вещества образуются только от двух- или полиосновных кислот: серной, фосфорной, угольной. Они относятся к неустойчивым соединениям и при нагревании происходит их разложение на составляющие элементы. В названии таких веществ всегда используют приставку «гидро», а если незамещенных атомов водорода осталось два — приставку «ди»:
- NaHSO4 — гидросульфат натрия.
- CaHPO4 — гидрофостфат кальция.
- KH2PO4 — дигидрофосфат калия.
Образование основных солей происходит при частичном замещении гидроксильных групп кислотными остатками, причем валентность основного остатка всегда будет равна числу замещенных гидроксильных групп. Номенклатура названий таких химических соединений образуется в зависимости от количества гидроксогрупп приставками «гидроксо» и «дигидроксо»:
- Аl (OH)SO4 — гидроксосульфит алюминия.
- Cu (OH)Cl — гидроксохлорид меди.
- Fe (OH)2NO3 — дигидроксохлорид железа.
Комплексные соединения и кристаллогидраты
Этот класс химических соединений отличается большим разнообразием. В изучении комплексных солей (КС) большую роль сыграли швейцарский ученый А. Вернер и русский химик немецкого происхождения В. Освальд. КС состоят из комплексных частиц. Центральный элемент в комплексе называется комплексообразователем, а связанные с ним элементы — лигандами. Их число — это координационное число соединения. Лигандами могут быть как нейтральные молекулы, так и разнообразные ионы и катион водорода H+.
КС так и классифицируются на нейтральные, анионные и катионные. Разными лигандами образуются такие группы химических веществ:
- амиакаты, в которых с комплексообразователем связаны молекулы аммиака — Cl3;
- аквакомплексы, образованные лигандами воды — Cl3;
- ацидокомплексы, включающие кислотные остатки — K2.
Кристаллы, образующиеся в водном растворе при выпадении в осадок солей, называются кристаллогидратами. При этом между молекулами воды и солевыми ионами формируются прочные связи, образующие кристаллическую решетку. Химические формулы кристаллогидратов записывают в виде количественного соотношения соли и воды, разделенных точкой — Na2SO4⋅10H2O. В номенклатуре для обозначения количества воды употребляются греческие числа — ди, три, тетра, гекса и так далее, с которых и начинается название. Число выступает приставкой к слову «гидро», а затем следует стандартное название соли: CaSO4⋅2H2O — дигидрат сульфата кальция.
Исторические наименования
Названия химических веществ соответствуют международной системе правил, позволяющей давать им названия, по которым можно правильно составить их формулу. Многие соединения солевой группы давно и хорошо известны, и в процессе их использования химики много лет назад уже как-то называли их. Традиционные или тривиальные названия полезно знать любому человеку. Их список приведен в таблице:
| Соль | Номенклатурное название | Тривиальное название |
| CuSO4⋅5H2O | Пентагидрат сульфата меди | Медный купорос |
| CaCO3 | Карбонат кальция | Известняк |
| AgNO3 | Нитрат серебра | Ляпис |
| NaHCO3 | Гидрокарбонат натрия | Питьевая сода |
| K2СO3 | Карбонат калия | Поташ |
| HgCl2 | Хлорид ртути | Сулема |
| Na2SiO3 | Силикат натрия | Жидкое стекло |
Физические свойства соли
Химия, как точная наука, вкладывает в название того или иного вещества всю возможную информацию о его составе и возможностях. Так, все наименования солей в современной интерпретации состоят из двух слов: одна часть имеет название металлического составляющего в именительном падеже, вторая — содержит описание кислотного остатка.
Эти соединения не имеют молекулярного строения, поэтому при обычных условиях они представляют собой твердые кристаллические вещества. Многие соли обладают кристаллической решеткой. Кристаллы этих веществ тугоплавки, поэтому для их плавления нужны очень высокие температуры. Например, сульфид бария плавится при температуре около 2200о С.
По растворимости соли делятся на растворимые, малорастворимые и нерастворимые. Примером первых могут служить хлорид натрия, нитрат калия. К малорастворимым относят сульфит магния, хлорид свинца. Нерастворимые – это карбонат кальция. Информация о растворимости того или иного вещества содержится в справочной литературе.
Рассматриваемый продукт химической реакции обычно не имеет запаха и обладает разным вкусом. Предположение о том, что все соли соленые — ошибочно. Чистый соленый вкус имеет только один элемент этого класса – наша старая знакома поваренная соль. Существуют сладкие соли бериллия, горькие – магния и безвкусные – например, карбонат кальция (мел обыкновенный).
Большинство данных веществ бесцветно, но среди них имеются и такие, которые имеют характерные окрасы. Например, железа (II) сульфат отличается характерным зеленым цветом, калия перманганат – фиолетовый, а кристаллы хромата калия – ярко-желтые.
Что такое соль?
Соль — это химическое соединение из отрицательных и положительных ионов. Попробуем образовать соль из иона олова(II) Sn2+ с хлорид-иона Cl—. Поскольку любая соль должно быть электрически нейтральным соединением, то суммарный заряд всех ее положительных и отрицательных ионов должен быть равным нулю. Поэтому соль, состоящая из ионов Sn2+ и Cl—, должна иметь молекулярную формулу SnCl2, а не SnCl или SnCl3. Это соединение называется хлорид олова(II). В случае с четырехвалентным ионом олова Sn4+, соединение имело бы вид SnCl4. Все просто!
Строго говоря, нельзя употреблять термины «молекулярная формула и молекулярная масса» соли, поскольку в солях нет молекул, а имеются только упорядоченные решетки, состоящие из ионов. Ни один из ионов натрия в структуре хлорида натрия, не «принадлежит» какому-либо конкретному хлорид-иону. Правильно говорить о химической формуле соли и соответствующей ей формульной массе. Поскольку химическая формула хлорида натрия — NaCl, то его формульная масса определяется как сумма атомных масс одного атома натрия Na и одного атома хлора Cl:
1 атом натрия: 22,990 а.е.м.
1 атом хлора: 35,453 а.е.м.
Итого: 58,443 а.е.м
Принято называть эту величину «молекулярной массой» хлорида натрия, и не возникает никаких недоразумений, если ясно отдавать себе отчет, какую структуру имеет соль. Моль хлорида натрия имеет массу 58,443 г. В нем содержится 6,022·1023 ионов натрия и 6,022·1023 хлорид-ионов. Хотя они и не объединены попарно в молекулы, соотношение между числом тех и других ионов точно 1:1.
Кристалл соли представляет собой устойчивое образование из катионов и анионов, в котором ион каждого типа как можно дальше удален от других ионов с зарядом такого же знака.
Если к кристаллу соли подвести БОЛЬШОЕ количество энергии, то можно разрушить такое идеальное расположение ионов в кристаллической решетке соли и позволить взаимно отталкивающимся зарядам приблизиться друг к другу на некоторый промежуток времени, тем самым разрушив устойчивую структуру кристалла. Как мы уже отметили, сообщаемая кристаллу соли энергия должна быть достаточно большой, по этой причине плавление солей происходит при бОльших температурах, чем у молекулярных кристаллов (например, лед).
Значение хлорида натрия для организма человека (adsbygoogle = window.adsbygoogle || []).push({});
Формула соли поваренной, ее состав приобрел жизненно важное значение для здоровья человека. Ионы натрия участвуют в передаче нервных импульсов
Анионы хлора необходимы для выработки соляной кислоты в желудке. Но слишком большое содержание поваренной соли в пище может приводить к высокому кровяному давлению и повышению риска развития заболеваний сердца и сосудов. В медицине при большой кровопотере пациентам вводят физиологический солевой раствор. Для его получения в одном литре дистиллированной воды растворяют 9 г хлорида натрия. Человеческий организм нуждается в непрерывном поступлении этого вещества с пищей. Выводится соль через органы выделения и кожу. Среднее содержание хлорида натрия в теле человека составляет примерно 200 г. Европейцы потребляют в день около 2-6 г поваренной соли, в жарких странах эта цифра выше в связи с более высоким потоотделением.
Значение хлорида натрия для организма человека
Формула соли поваренной, ее состав приобрел жизненно важное значение для здоровья человека. Ионы натрия участвуют в передаче нервных импульсов
Анионы хлора необходимы для выработки соляной кислоты в желудке. Но слишком большое содержание поваренной соли в пище может приводить к высокому кровяному давлению и повышению риска развития заболеваний сердца и сосудов. В медицине при большой кровопотере пациентам вводят физиологический солевой раствор. Для его получения в одном литре дистиллированной воды растворяют 9 г хлорида натрия. Человеческий организм нуждается в непрерывном поступлении этого вещества с пищей. Выводится соль через органы выделения и кожу. Среднее содержание хлорида натрия в теле человека составляет примерно 200 г. Европейцы потребляют в день около 2-6 г поваренной соли, в жарких странах эта цифра выше в связи с более высоким потоотделением.
Классификация соли
Химия разделяет все виды неорганических солей на несколько основных признаков. Соли, получающиеся при полном замещении водорода в кислоте, называют нормальными или средними. Например, сульфат кальция.
Вдоль шагов некоторых конструкций, аранжировок и деревянных установок в основном течении Сраратского потока было обнаружено несколько «горных молотков»? и фрагмент топора, сделанный из камня. В то же время, серия образцов из следов деревянных конструкций была собрана в русле реки Сраат. Каменные инструменты, используемые шахтерами.
Презентация археологических открытий. До настоящего времени было исследовано 20 археологических разрезов. Было обнаружено много следов обработанной древесины, в том числе следы части деревянной конструкции. Один из руководителей «трофея»? вся длина была закрыта, а другая открыта. В этих отверстиях были вставлены прорези из ветвей деревьев с центрально-продольными отверстиями. Значительно ли, что в закрытом конце «переезды»? они имели на каналах истребителя, выгравированных вокруг ствола, очевидно, предназначенных для фиксации струн, с которыми они были приостановлены.
Соль, которая является производной от реакции неполного замещения, называется кислой или основной. Примером такого образования может быть реакция гидросульфата калия: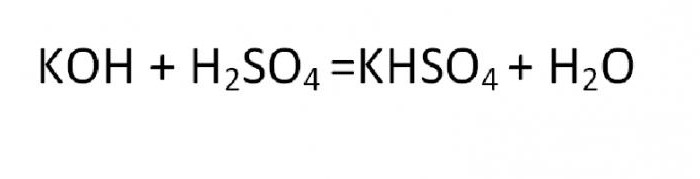
Основная соль получается при такой реакции, в которой гидроксогруппа не полностью замещается на кислотный остаток. Вещества данного вида могут быть образованны теми металлами, чья валентность равна двум или больше. Типичная формула соли этой группы может быть выведена из такой реакции:
В восточной части С. 1 была обнаружена массивная четырехугольная конструкция из деревянных балок, которые были установлены друг на друга. Внутри этого здания были два круговых луча, которые пересекались перпендикулярно друг другу. По всей вероятности, эта конструкция представляет собой следы «колодца»? Вставка в шахту.
Рядом с массивным деревянным зданием была обнаружена деревянная лестница, хорошо сохранившаяся. Поскольку археологические исследования не были завершены, площадь была сохранена с постоянным слоем земли. В будущих исследованиях будет представлена информация о функциональности этих установок и конструкций из цельного дерева.
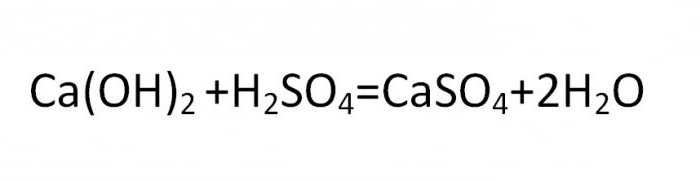
Нормальные, средние и кислые химические соединения образуют классы солей и являются стандартной классификацией этих соединений.
Природные месторождения
Среди мест, характеризующихся большими запасами поваренной соли, выделим:
- Артемовское месторождение, расположенное в Донецкой области. Здесь осуществляется добыча соли шахтовым способом;
- озеро Баскунчак, перевоз ведется по специально построенной железной дороге;
- калийные соли в большом количестве обнаружены в Верхнекамском месторождении, где шахтовым способом идет добыча этого полезного ископаемого;
- в Одесских лиманах велась добыча до 1931 года, в настоящее время месторождение не используется в промышленных объемах;
- в Сереговском месторождении проводится выпаривание рапы.
Растворы кислых солей
Кислые соли в растворе распадаются на сложные отрицательные ионы, представляющие собой кислотный остаток, и простые анионы, являющиеся положительно заряженными частицами металла.  Например, реакция растворения гидрокарбоната натрия ведет к распаду соли на ионы натрия и остаток НСО 3 — .
Например, реакция растворения гидрокарбоната натрия ведет к распаду соли на ионы натрия и остаток НСО 3 — .
Пока неизвестно, являются ли эти объекты современными или нет современными деревянными конструкциями и фитингами. Пока что в отношении назначения и хронологического построения этих молотков у нас нет других данных, кроме аналогов, которые существуют в других местах.
Археологический объект Бэиле Фига, в свете полученных до сих пор результатов, представляется наиболее релевантным в Трансильвании и одним из самых важных в Румынии в отношении доисторической эксплуатации соли. Знакомства ок. 40 образцов древесины с использованием метода С14, выполненных в престижных лабораториях Грёнингена, Гейдельберга и Оксфорда, а также дендрокронологических исследований ок. 80 стволов деревьев, проведенных в Корнельском университете, подчеркнули следующие археологические последовательности.
Полная формула выглядит таким образом: NaHCO 3 = Na + + HCO 3 — , HCO 3 — = H + + CO 3 2- .
Излишек соли в организме
Натрий нормализует функцию почек, поддерживает в норме водно-солевой баланс, нервно-мышечную деятельность, участвует в сокращении мышц, транспорте сахара крови в клетки. Без данного элемента невозможен рост организма, нормальное функционирование внутренних органов .
Вступая во взаимодействие с хлором, натрий противостоит утечке жидкости из кровеносных сосудов в близлежащие ткани. Переоценить роль данного элемента для живого организма невозможно .
У здорового человека содержание натрия в крови варьируется в диапазоне от 135 до 145 миллимолей на литр. Смещение данного равновесия в большую или меньшую сторону указывает на наличие «скрытых» проблем в организме .
При длительном избыточном потреблении соли (свыше 10 – 15 грамм в день) развивается гипернатриемия, сопровождающаяся клеточной дегидратацией .
Другие причины накопления натрия в организме:
- сахарный диабет 2 типа;
- гипертония;
- неправильное питание (неконтролируемое употребление фастфуда, полуфабрикатов);
- наследственная предрасположенность;
- недостаточное количество потребляемой воды (меньше 1,5 литра в сутки);
- прием минеральный препаратов;
- нарушение водно-солевого обмена;
- дисфункция надпочечников, почек .
Симптомы излишка:
- задержка жидкости в организме (возникновение отеков);
- повышение температуры тела;
- чрезмерная возбудимость;
- снижение функции почек;
- постоянная жажда;
- вялость, упадок сил;
- запор;
- боли в суставах;
- моча темно-желтого цвета;
- частые головные боли;
- судороги мышц;
- двигательное беспокойство;
- артериальная гипертензия .
Последствия:
- растягиваются мышечные волокна, ослабляется их функция (ухудшается реакция на импульсы);
- развивается почечная недостаточность, нефрит, воспаление каналов;
- загущается кровь, учащается пульс, появляется хроническая гипертония;
- повышается риск инсульта, инфаркта;
- развиваются аритмия, тахикардия;
- появляются жировые отложения (бляшки) на стенках сосудов;
- снижается регуляторная функции гипоталамуса .
Для устранения симптомов гипернатриемии и улучшения состояния больного следует строго контролировать количество употребляемой соли и снизить ее до критического минимум 3 – 5 грамм в день. Кроме того, назначается строгая диета, медикаментозное, амбулаторное лечение. Цель терапии – усиленное выведение и блокировка отложения соли .
Польза в хозяйстве
Хлористый натрий используют в быту в следующих целях:
- чтобы при варке не трескалась скорлупа на яйцах (добавить в воду);
- чтобы в духовом шкафе не пригорело печенье (насыпать под формочки);
- чтобы не заводились жучки в банках с крупами (положить на дно емкости пакетик с солью);
- для выведения жирных пятен с одежды (натереть солью);
- для устранения запаха тины от рыбы (прополоскать в насыщенном соляном растворе);
- чтобы цветное белье во время стирки не полиняло (добавить в воду);
- чтобы первый блин вышел «не комом» (протереть сковороду);
- чтобы сухие грибы приобрели былой вид (вымачивать в соленом молоке);
- чтобы сырые дрова разгорались скорее (посыпать кристаллами);
- для придания мягкости махровым халатам и полотенцам (после стирки прополосните в воде с добавлением соли).
Определение соли
Четкий ответ на вопрос, что такое соль, можно найти в трудах М. В. Ломоносова. Такое имя он присвоил хрупким телам, которые могут растворяться в воде и не воспламеняются под воздействием высоких температур или открытого огня. Позднее определение выводили не из их физических, а из химических свойств данных веществ.
Все это предназначалось для удаления Злобных Вульпов, которые могли бы принести несчастье. Вот почему, со временем, почти каждая шахта приобрела часовню, место молитвы для них. В Прайде есть экуменическая церковь, в которой трое деноминированных молельней молились в Дедже-православном, а в Польше в Величке — настоящий собор, выкопанный в соль интеллектуалов, которые были выброшены коммунистическим режимом.
Румынская соль рискует покинуть государственный контроль, генеральный секретарь Консультативного совета по деловой среде Ионел Бланкулеску обратил внимание на «предупреждающий знак» премьер-министра Румынии. Наша соль находится в большой опасности потеряться под контролем государства
К этим странам относятся Германия и Австрия. Директива не распространяется на Румынию, поскольку наша соль имеет другую химическую формулу. Вот почему наша страна стала «солью Эльдорадо».
Школьные учебники неорганической химии дают достаточно ясное понятие того, что такое соль. Так называются продукты замещения химической реакции, при которой атомы водорода кислоты в соединении замещаются на металл. Примеры типичных соединений солей: NaCL, MgSO 4 . Легко увидеть, что любую эту запись можно разделить на две половины: в левой составляющей формулы всегда будет записан металл, а в правой — кислотный остаток. Стандартная формула соли выглядит следующим образом:
Трансильвания, почти все, сидит на соляной плите, оставленной здесь после вод Тити. Было обнаружено, что первые подвиги соли были сделаны Гета, где-то в Долине цветов, недалеко от Клужа. Когда пришли римляне, они подняли эксплуатацию на другой уровень, совершили торговлю солью, сделали дороги и замки возле полей, сделали законы соли. С течением времени слово зарплата оставалась, потому что солдаты, работающие на соль, получали зарплату в кусках или соленых пельменях. Соль из Трансильвании обеспечивала население севернее и южнее Дуная.
В то время это было очень необходимо, оно использовалось для подготовки шкур, сохранения пищи и кормления животных. Она также отличала людей: только богатые имели соль на столе. Это считалось белым золотом древнего мира. Известно, что в Трансильвании созревает древняя соляная дорога, согласно монографии «Время, соль и человек», которую вы можете прочитать здесь частично.
Me n m Кислотный остаток m n .
Соль и пищеварительная система
Задумывались ли вы о том, почему рецепты сладких блюд часто содержат совсем незначительное количество соли? Ведь многим из нас больше нравится вкус сахара? Тем не менее, именно хлорид натрия способен активизировать уникальный фермент птиалин во рту человека. Активация этого энзима означает готовность рецепторов пищи воспринимать вкус еды. Т.е. вкус блюда, в котором присутствует хлорид натрия, будет казаться нам более ярким.

Поскольку NaCl входит в большинство покупаемых в готовом виде продуктов и тех блюд, которые мы готовим сами, можно предположить, что дефицит соли в организме может возникнуть в исключительных случаях, возможно при частой сильной рвоте, при диарее, при чрезмерном потоотделении.
Заподозрить дефицит минерала в организме можно в случае:
быстрой утомляемости,
частого повторения мышечных судорог,
головокружений,
ощущения тошноты,
рассеянности и невозможности сконцентрировать внимание на определенном вопросе.
Опасным для человека может быть употребление слишком большого количества чистой воды. Наступающая при этом гипонатриемия заключается в том, что в следствии снижения количества NaCl, в организме перестает удерживаться вода. Такая ситуация крайне негативно сказывается на сердечно-сосудистой системе человека и может закончиться летальным исходом.
Краткое описание
Все соли (формула — MnAcm) обладают сложным химическим составом, из-за чего могут быть неорганическими либо органическими. Эти вещества получили огромный спрос в разных отраслях современной промышленности. В теоретической химии соли принято разделять сразу на несколько групп:
- Состоящие из анионов и катионов. Речь касается электрической диссоциации.
- Сложные химические соединения могут быть образованы одним либо сразу несколькими кислотными остатками, а также ионом металла.
- Соли могут формироваться в результате взаимодействия кислот и оснований.
К кислотным остаткам помимо металлов могут присоединяться ионы гидроксония, аммония, а также фосфония. В большинстве случаев MnAcm являются твёрдыми кристаллами. Науке известны соли разного цвета (например, зелёные, фиолетовые, белые). Прозрачные кристаллы свойственны для NaCl.
Строение солей отличается наличием кристаллической решётки, которая содержит анионы, а также катионы. Есть и другой вариант. В бесконечную цепочку соединены фрагменты анионов из кислотных остатков. В трёхмерных полостях расположены катионы. Такая структура свойственна силикатам, что отражается на их итоговых характеристиках: неспособность проводит ток и высокая температура плавления.
Технология добычи
- Выпаривание из воды естественным способом, в специальных резервуарах. Такая соль богата микроэлементами, особенно йодом. Содержание NaCl – 94-98%.
- Добыча из недр земли путем разработки шахт или карьеров. Эта соль практически не содержит примесей и влаги. Содержание NaCl – 98-99%.
- Добыча путем вымывания рассола, с последующим выпариванием. Так добывается выварочная соль с мелкими кристалликами и с наилучшей степенью очистки — соль «Экстра». Содержание NaCl 98-99,8%.
- Собирание солесосом со дна соляных озер. Самосадочная соль содержит значительное количество микроэлементов. Содержание NaCl – 94-98%.


